DIANEAL FOR PERITONEAL DIALYSIS- anhydrouse dextrose, sodium chloride, sodium lactate, calcium chloride, magnesium chloride injection, solution
Baxter Healthcare Corporation
Disclaimer: This drug has not been found by FDA to be safe and effective, and this labeling has not been approved by FDA. For further information about unapproved drugs, click here.
----------
DIANEAL® SOLUTION FOR PERITONEAL DIALYSIS
IMPORTANT DRUG INFORMATION
October 2014
Subject: Temporary Importation of DIANEAL® Solution for Peritoneal Dialysis
Dear Healthcare Professional,
Due to current critical shortage of Dianeal peritoneal dialysis solutions for new and existing patients in the US market, Baxter Healthcare Corporation (Baxter) is coordinating with the Food and Drug Administration (FDA) to increase the availability of the drug. Baxter has initiated temporary importation of Dianeal peritoneal dialysis solutions manufactured at Baxter’s Castlebar, Ireland facility and marketed within the European Union (EU). The FDA has not approved this product in the United States.
Prior to its use, it is important to check for leaks by squeezing the inner bag firmly. If leaks are found, do not use solution as sterility may be impaired. Additionally, check to see that solution is clear and free of foreign matter. Solutions that are cloudy, discolored, contain visible particulate matter, or show evidence of leakage should not be used or discarded, but reported to Baxter Product Surveillance immediately. To report product quality issues, please contact Baxter Product Surveillance at 1-800-437-5176.
There are no clinically relevant differences in the composition of the European-manufactured product and the US-manufactured product (see Table 1). However, because the imported product is only available in one size (5000 ml), the number of solution bags patients use per treatment may require modification. Although the frangible, medication ports, and connection caps may appear different for the European-manufactured product, they function in a similar manner to the US-manufactured product.
Effective immediately, Baxter will offer DIANEAL PD4 Glucose Solution for Peritoneal Dialysis in flexible polyvinyl chloride bag containers in the following volume:
Automated Peritoneal Dialysis (APD) product, 5000mL container:
|
||
|
Product* |
|
|
|
Dianeal PD4 Glucose 1,36% w/v 13,6 mg/ml Solution for Peritoneal Dialysis |
|
|
|
Dianeal PD4 Glucose 2,27% w/v |
|
|
|
Dianeal PD4 Glucose 3,86% w/v |
|
|
At this time, importation or distribution of Dianeal peritoneal dialysis solution in the United States by any entity other than Baxter or its authorized distributor(s) is considered a violation of the Federal Food, Drug and Cosmetic Act and is subject to enforcement by the FDA.
Dosage and Administration
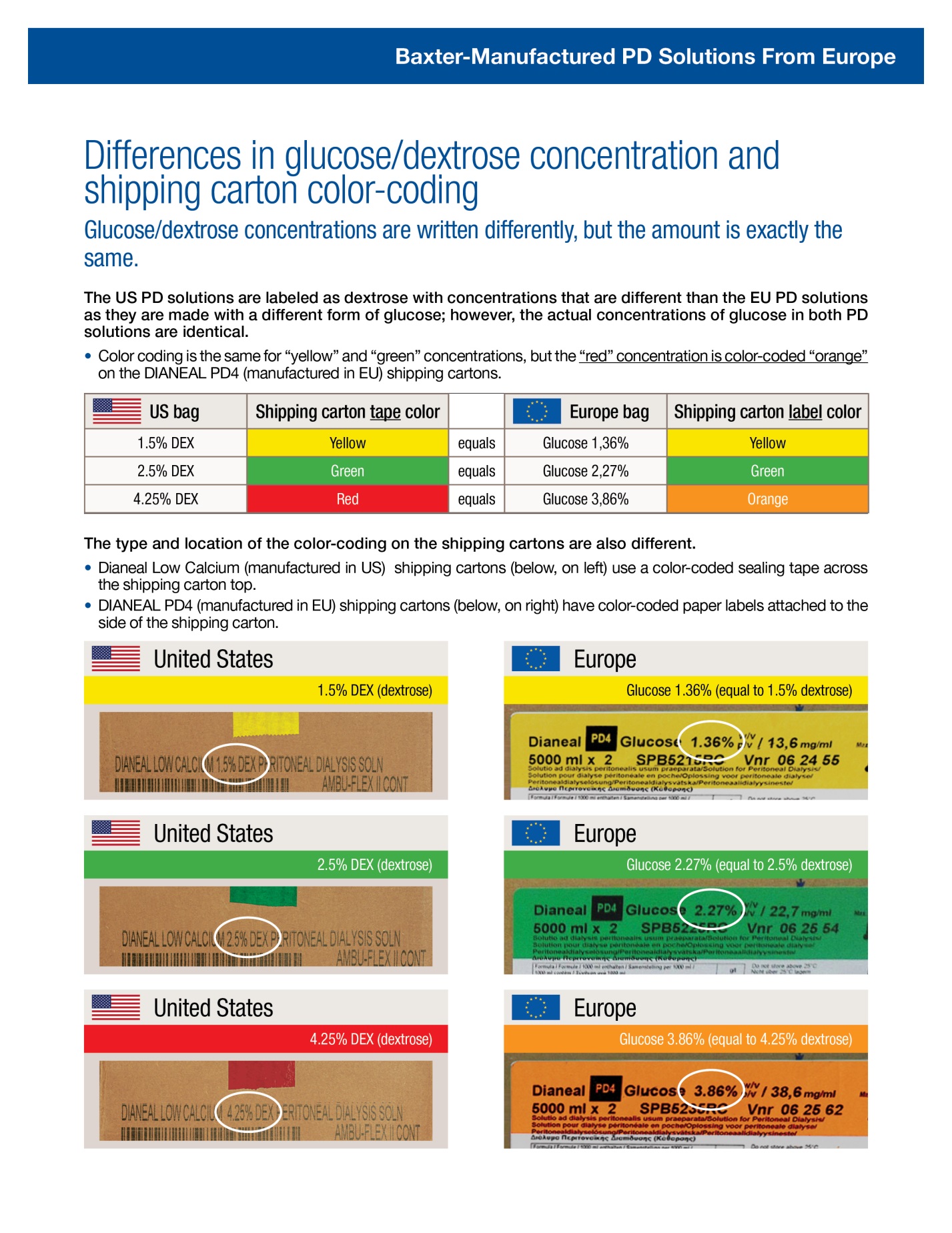
Baxter’s DIANEAL PD4 with 1,36%, 2,27%, or 3,86% Glucose Solution for Peritoneal Dialysis (manufactured in EU) has the same ionic composition as Baxter’s Dianeal Low Calcium (2.5 mEq/L) Peritoneal Dialysis Solution with 1.5%, 2.5%, or 4.25% Dextrose products (manufactured in US). Please note that numerical values for EU products use commas in place of decimal points for the US products. Dianeal solution concentration is expressed as % anhydrous glucose, which correlates to the following % dextrose monohydrate equivalents:
- • 1.5% dextrose monohydrate (or glucose monohydrate) = 1,36% anhydrous dextrose (or anhydrous glucose)
- • 2.5% dextrose monohydrate (or glucose monohydrate) = 2,27% anhydrous dextrose (or anhydrous glucose)
- • 4.25% dextrose monohydrate (or glucose monohydrate) = 3,86% anhydrous dextrose (or anhydrous glucose)
As such, clinical practice for usage, administration, and dosage for DIANEAL PD4 with 1,36%, 2,27%, or 3,86% Glucose Solution for Peritoneal Dialysis (manufactured in EU) products is the same as with the Dianeal Low Calcium (2.5 mEq/L) Peritoneal Dialysis Solution with 1.5%, 2.5%, or 4.25% Dextrose products (manufactured in US). Please refer to the FDA-approved Dianeal Low Calcium (2.5 mEq/L) Peritoneal Dialysis Solution US Package Insert for reference.
Summary of Product Differences
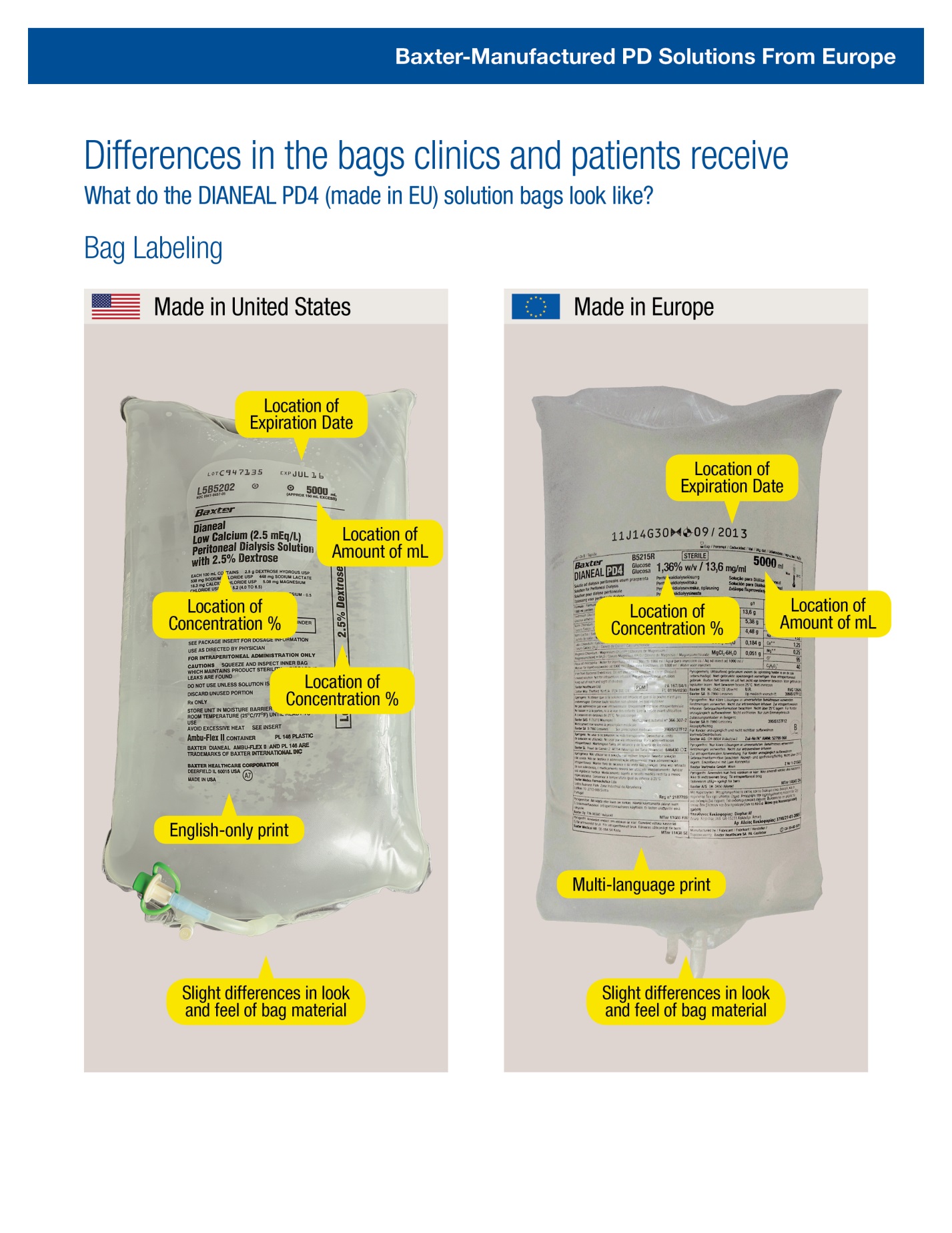
Before prescribing, healthcare providers should be aware of some key differences in the container packaging and labeling between the DIANEAL PD4 with Glucose Solution for Peritoneal Dialysis products (manufactured in EU) and Dianeal Low Calcium (2.5 mEq/L) Peritoneal Dialysis Solution with Dextrose (manufactured in US).
Key differences are highlighted in the attached Product Comparison Tables as follows:
- • Table 1: Dianeal Formulation Comparison (as labeled)
- • Table 2: Comparison of Dianeal container labels for APD, 5000 mL
Additional differences with photographs are highlighted in the accompanying Comparison Guide, which describes differences in shipping cartons, solution bags, and labeling.
Important Notes
- • Despite visual differences in the product appearance, the Luer-lock connector is the same and is fully compatible with peritoneal dialysis sets marketed in the United States.
- • Prior to use, it is important to check for leaks by squeezing the inner bag firmly. If leaks are found, do not use solution as sterility may be impaired. Additionally, check to see that solution is clear and free of foreign matter. Solutions that are cloudy, discolored, contain visible particulate matter, or show evidence of leakage should not be used or discarded, but reported to Baxter Product Surveillance immediately. To report product quality issues, please contact Baxter Product Surveillance at 1-800-437-5176.
- • DIANEAL PD4 with Glucose Solutions imported product and carton labeling includes barcodes; however, the barcodes may not register accurately in the US scanning systems. Institutions should manually input the product into their systems and confirm that barcode systems do not provide incorrect information when the product is scanned. Alternative procedures should be followed to assure that the correct drug product is being used and administered to individual patients.
If you have any questions about the information contained in this letter or the use of DIANEAL PD4 with 1,36%, 2,27%, or 3,86% Glucose Solution for Peritoneal Dialysis products, please contact Baxter’s Medical Information Service at 1-888-736-2543, Option #2. To place an order, please contact Baxter’s Center for Service by calling 1-888-229-0001.
To report product quality issues, please contact Baxter Product Surveillance at 1-800-437-5176. To report adverse events associated with Dianeal peritoneal dialysis solutions, please call Baxter at 1-866-888-2472 or fax: 1-800-759-1801. Adverse events that may be related to the use of this product may also be reported to the FDA’s MedWatch Adverse Event Reporting program either online, by regular mail or by fax.
- • Online:www.fda.gov/medwatch/report.htm
- • Regular Mail: use postage-paid FDA form 3500 available at:
- www.fda.gov/MedWatch/getforms.htm. Mail to MedWatch 5600 Fishers Lane, Rockville, MD 20852-9787
- • Fax: 1-800-FDA-0178 (1-800-332-0178)
Sincerely,
Mary Gellens, M.D.
Baxter Healthcare Corporation
Baxter and Dianeal are registered trademarks of Baxter International Inc.
Baxter Healthcare Corporation
One Baxter Parkway
Deerfield, Illinois 60015
USMP/76/14-0013 10/2014
|
||
|
Product manufactured in EU |
Product manufactured in US |
|
|
Product name |
DIANEAL PD4 Glucose Solution for Peritoneal Dialysis |
Dianeal Low Calcium (2.5 mEq/L) Peritoneal Dialysis Solution with Dextrose |
|
Content |
1,36% w/v / 13,6 mg/ml |
1.5% Dextrose |
|
2,27% w/v / 22,7 mg/ml Formula / 1000 ml:
|
2.5% Dextrose |
|
|
3,86% w/v / 38,6 mg/ml Formula / 1000 ml: |
4.25% Dextrose
Each 100 mL contains:
|
|
|
Ionic composition* |
Sodium 132 mmol/L |
Sodium 132 mEq/L |
|
Osmolarity (calculated) |
1,36% Glucose: 344 mOsm/L 2,27% Glucose: 395 mOsm/L 3,86% Glucose: 483 mOsm/L |
1.5% Dextrose: 344 mOsmol/L |
|
Storage conditions |
Do not store above 25°C. |
It is recommended the product be stored at room temperature (25°C /77°F): brief exposure up to 40°C (104°F) does not adversely affect the product. |
PACKAGE/LABEL PRINCIPAL DISPLAY PANEL
Lot / Ch B / Παρτίδα Exp / Pérempt / Caducidad / Val / Utg dat / Udløbsdato / Verw bis / Λήξη
BaxterB5215R STERILE 5000 ml
DIANEAL PD4 1,36% w/v / 13,6 mg/ml Max 25°C
Glucose
Glucosa
Solutio ad dialysis peritonealis usum praeparata
Solution for Peritoneal Dialysis
Solution pour dialyse péritonéale en poche
Oplossing voor peritoneale dialyse
Peritonealdialyselösung
Peritonealdialysvätska
Peritonealdialysevæske, opløsning
Peritoneaalidialyysineste
Solución para Diálisis Peritoneal
Διάλυμα Περιτοναϊκής Διαπίδυσης (Κάθαρσης)
Formula / Formule / 1000 ml enthalten / Samenstelling per 1000 ml /
Composición por 1000 ml / Σύνθεση ανά 1000 ml g/l
Dextrosum (Glucosum) Anhydricum / Anhydrous Glucose / Glucose anhydre /
Glucosa anhidra / Glucose wasserfrei / Watervrije glucose C6H12O613,6 g
Natrii Chloridum / Sodium Chloride / Chlorure de Sodium / Natriumchlorid /
Cloruro Sódico / Natriumchloride NaCl 5,38 g
Natrii Lactas / Sodium Lactate / Lactate de Sodium / Natrium L (+) Lactat / Lactato Sódico /
Natriumlactaat C3H5NaO3 4,48 g
Calcii Chloridum / Calcium Chloride / Chlorure de Calcium dihydraté / Calciumchlorid • 2H2O /
Cloruro Cálcico 2H2O / Calciumchloridedihydraat CaCl2·2H2O 0,184 g
Magnesii Chloridum / Magnesium Chloride / Chlorure de Magnésium hexahydraté /
Magnesiumchlorid • 6H2O / Cloruro Magnésico 6H2O / Magnesiumchloridehexahydraat
MgCl2·6H2O 0,051 g
Aqua ad iniectabilia / Water for Injections ad / eau pour préparations injectables qsp 1000 ml / to 1000 ml / Agua para inyección cs /
Aq ad iniect ad 1000 ml / Wasser für Injektionszwecke ad 1000 ml / Water voor injecties ad 1000 ml
Osmolarity / Osmolarité /
Osmolaridad / Osmolaridade /
berechnete Osmolarität / Osmolarit / Osmolariteit /
Ωσμωτικότητα 344 mOsm/l
mmol/l
Na+ 132
Ca++ 1,25
Mg++ 0,25
Cl- 95
C3H5O3- 40
Free from Bacterial Endotoxins Do not use unless solution is clear
Do not store above 25°C For immediate use Discard any unused
solution Not for intravenous infusion For intraperitoneal infusion
Keep out of reach and sight of children PA 167/84/1
Baxter Healthcare LtdPOM PL 00116/0230
Caxton Way Thetford Norfolk IP24 3SE UK MA 161/01104
Pyrogeenvrij Uitsluitend gebruiken indien de oplossing helder is en de zak onbeschadigd
Niet-gebruikte oplossingen vernietigen Voor intraperitoneaal gebruik
Buiten het bereik en uit het zicht van kinderen bewaren Voor gebruik de bijsluiter lezen
Niet bewaren boven 25°C Niet invriezen
Baxter BV NL-3542 CE Utrecht UR RVG 12609
Baxter SA B-7860 Lessines Op medisch voorschrift 395IS127F12
Apyrogène N’utiliser que si la solution est limpide et que si la poche
n’est pas endommagée Eliminer toute solution non utilisée
Ne pas réutiliser Ne pas administrer par voie intraveineuse
Uniquement par voie intrapéritonéale Tenir hors de la portée et de la
vue des enfants Lire la notice avant utilisation
Ne pas conserver au-dessus de 25°C Ne pas congeler
Titulaire Baxter SAS 6 av L Pasteur F-78310 Maurepas
- Médicament autorisé n° 3400936630727
Médicament non soumis à prescription médicale
Baxter SA B-7860 Lessines
Sur prescription médicale 395IS127F12
Pyrogenfrei Nur klare Lösungen in unversehrten Behältnissen verwenden
Restmengen verwerfen Nicht zur intravenösen Infusion Zur intraperitonealen Infusion Gebrauchsinformation beachten Nicht über 25°C lagern
Für Kinder unzugänglich aufbewahren Nicht einfrieren Nur zum Einmalgebrauch
Zulassungsinhaber in Belgien:
Baxter SA B-7860 Lessines Rezeptpflichtig 395IS127F12
Für Kinder unzugänglich und nicht sichtbar aufbewahren
Vertrieb/Distribution: m
Baxter AG CH-8604 Volketswil Zul-Nr/N° AMM: 52799 066 B SWISSmedic Logo
Apirógeno No usar si la solución no está transparente
Desechar el resto de solución no utilizada No usar por vía intravenosa
Para administración intraperitoneal
Manténgase fuera del alcance y de la vista de los niños
Baxter SL
Pouet de Camilo 2 46394 Ribarroja del Turia (Valencia)
- 646430
Pyrogenfrei Achtung: Dieses Arzneimittel kann die Reaktionsfähigkeit und
Verkehrstüchtigkeit beeinträchtigen Nur klare Lösungen in unversehrten
Behältnissen verwenden Restmengen verwerfen Nicht zur intravenösen Infusion
Zur intraperitonealen Anwendung Arzneimittel für Kinder unzugänglich aufbewahren
Packungsbeilage beachten Rezept- und apothekenpflichtig Nicht über 25°C lagern
In der Originalverpackung aufbewahren Enizelbeutel mit Luer-Konnektor
Pharmazeutischer Unternehmer: Baxter Healthcare GmbH 1020 Wien Z Nr 1-21583
Pyrogeeniton Älä käytä ellei liuos ole kirkas
Hävitä käyttämättä jäänyt liuos Ei laskimoinfuusioon
Intraperitoneaaliseen käyttöön Ei lasten ulottuville eikä näkyville
- Baxter Oy FIN-00381 Helsinki MTnr 11086 FIN
Pyrogenfri Anvendes kun hvis væsken er klar Ikke anvendt væske skal kasseres
Ikke til indtravenøs brug Til intraperitoneal brug Opbevares utilgængeligt for børn
Baxter A/S DK-3450 Allerød MTnr 14645 DK
Pyrogenfri Användes endast om vätskan är klar
Oanvänd vätska kasseras Ej för intravenöst bruk
För intraperitonealt bruk Förvaras oåtkomligt för barn
Baxter Medical AB SE-164 94 Kista MTnr 11438 SE
Mη πυρετoγóνo Mη χρησιμoπoιεíτε εκτóς εάν τo διάλυμα εíναι διαυγές και o περιέκτης δεν έχει
υπoστεí ζημιά Φυλάσσεται σε θερμοκρασία μικρότερη των 25°C Aπoρρíψτε την αχρησιμoπoíητη
πoσóτητα Όχι για ενδoφλέβια έγχυση Για ενδoπεριτoναϊκή έγχυση Φυλάσσεται σε μέρος το οποίο
δεν βλέπουν και δεν προσεγγίζουν τα παιδιά Móνo για Noσoκoμειακή χρήση
Κάτοχος Αδείας Κυκλοφορίας Baxter S p A Piazzale dell’ Industria 20 IT-00144 Roma Italy
Αρ Αδεíας Κυκλoφoρíας: 40850/14-09-2009
TRK500198 B
CB-35-03-351
-
Dianeal PD4 Glucose 1.36% w/v p/v 13,6 mg/ml
5000 ml x 2 SPB5215RC Vnr 06 24 55
Solutio ad dialysis peritonealis usum praeparata/Solution for Peritoneal Dialysis/
Solution pour dialyse péritonéale en poche/Oplossing voor peritoneale dialyse/
Peritonealdialyselösung/Peritonealdialysvätska/Peritoneaalidialyysineste/
Διάλυμα Περιτοναϊκής Διαπίδυσης (Κάθαρσης)
Formula / Formule / 1000 ml enthalten / Samenstelling per 1000 ml /
1000 ml contém /Σύνθεση ανά 1000 – g/l
Dextrosum (Glucosum) Anhydricum/Anhydrous Glucose/Glucose
anhydre/Glucose anidra/Glucose wasserfrei/Watervrije glucose – 13,6 g
Natrii Chloridum/Sodium Chloride/Chlorure de Sodium/
Natriumchlorid/Cloreto de Sódio/Natriumchloride – 5,38 g
Natrii Lactas/Sodium Lactate/Lactate de Sodium/
Natrium L(+) Laktat/Lactato de sódio/Natriumlactaat – 4,48 g
Calcii Chloridum/Calcium Chloride/Chlorure de Calcium dihydraté/
Calciumchlorid·2H O/Cloreto de Cálcio/Calciumchloridedihydraat – 0,184 g
Magnesii Chloridum/Magnesium Chloride/Chlorure de Magnésium
hexahydraté/Magnesiumchlorid·6H O/Cloreto de Magnésio/
Magnesiumchloridehexahydraat – 0,051 g
Aqua ad iniectabilia/Water for Injections ad/eau ppi/to 1000 ml/
Aq. ad iniect. ad 1000 ml/Wasser für Injektionszwecke ad 1000 ml/
Água para Injectáveis qb 1000 ml/Water voor injecties ad 1000 ml
PA 167/84/1
PL 00116/0230
MA 161/01104
Z.Nr.: 1-21583
RVG 12609
395IS127F12
MTnr 11438 SE
MTnr 11086 FIN
Médicament autorisé
n° 3400936630727
Αρ. Αδείας Κυκλοφορίας:
40850/14-09-2009
Zur intraperitonealen Anwendung. Packungsbeilage beachten.
Arzneimittel für Kinder unzugänglich aufbewahren. Achtung.
Dieses Arzneimittel kann die Reaktionsfähigkeit und Verkehrstüchtiglkeit
beeinträchtigen. Nur klare Lösungen in unversehrten. Behältnissen verwenden.
Restmengen verwerfen. Nicht zur intravenösen Infusion.
Pharmazeutischer Unternehmer: Baxter Healthcare GmbH, 1020 Wien.
rezept- und apothekenpflichtig. Steril, pyrogenfrei.
France: Médicament non soumis à prescription médicale
BE : Sur prescription médicale. Op medisch voorschrift. Rezeptpflichtig.
NL : U.R.
Παρτίδα:
Lot/Ch.B.:
Λήξη
Exp./Pérempt/
Val./Verw.bis/
Utg.dat.:
Max. 25°C
Do not store above 25°C
Nicht über 25°C lagern
In der Originalverpackung aufbewahren
Ne pas conserver au-dessus de 25°C
Säilytä alle 25°C
Bewaren beneden 25°C
Förvaras under 25°C
m/Skruvkoppling
Kierrekytkentä
Single bag with Luer connector
Einzelbeutel mit Luer-Konnektor
Poche simple - Connecteur luer
Enkele zak met luer-connector
Movός σάκος - Σύνδεσμος Luer
Zul.-Nr./N° AMM.:
52799 066
88-46-11-840
Bar Code
7 046260 624559
Bar Code
(01)03400936630727 (17)000000 (10)??????????
Vnr 06 24 55
Dianeal PD4 Glucose
1.36% w/v p/v 13,6 mg/ml
Παρτίδα:
Lot/Ch.B.:
SPB5215RC
5000 ml x 2
PACKAGE/LABEL PRINCIPAL DISPLAY PANEL
Lot / Ch B / Παρτίδα Exp / Pérempt / Caducidad / Val / Utg dat / Udløbsdato / Verw bis / Λήξη
BaxterB5225R STERILE 5000 ml
DIANEAL PD4 2,27% w/v / 22,7 mg/ml Max 25°C
Glucose
Glucosa
Solutio ad dialysis peritonealis usum praeparata
Solution for Peritoneal Dialysis
Solution pour dialyse péritonéale en poche
Oplossing voor peritoneale dialyse
Peritonealdialyselösung
Peritonealdialysvätska
Peritonealdialysevæske, opløsning
Peritoneaalidialyysineste
Solución para Diálisis Peritoneal
Διάλυμα Περιτοναϊκής Διαπίδυσης (Κάθαρσης)
Formula / Formule / 1000 ml enthalten / Samenstelling per 1000 ml /
Composición por 1000 ml / Σύνθεση ανά 1000 ml g/l
Dextrosum (Glucosum) Anhydricum / Anhydrous Glucose / Glucose anhydre /
Glucosa anhidra / Glucose wasserfrei / Watervrije glucose C6H12O6 22,7 g
Natrii Chloridum / Sodium Chloride / Chlorure de Sodium / Natriumchlorid /
Cloruro Sódico / Natriumchloride NaCl 5,38 g
Natrii Lactas / Sodium Lactate / Lactate de Sodium / Natrium L (+) Lactat / Lactato Sódico /
Natriumlactaat C3H5NaO3 4,48 g
Calcii Chloridum / Calcium Chloride / Chlorure de Calcium dihydraté / Calciumchlorid • 2H2O /
Cloruro Cálcico 2H2O / Calciumchloridedihydraat CaCl2·2H2O 0,184 g
Magnesii Chloridum / Magnesium Chloride / Chlorure de Magnésium hexahydraté /
Magnesiumchlorid • 6H2O / Cloruro Magnésico 6H2O / Magnesiumchloridehexahydraat
MgCl2·6H2O 0,051 g
Aqua ad iniectabilia / Water for Injections ad / eau pour préparations injectables qsp 1000 ml / to 1000 ml / Agua para inyección cs /
Aq ad iniect ad 1000 ml / Wasser für Injektionszwecke ad 1000 ml / Water voor injecties ad 1000 ml
Osmolarity / Osmolarité /
Osmolaridad / Osmolaridade /
berechnete Osmolarität / Osmolarit / Osmolariteit /
Ωσμωτικότητα 395 mOsm/l
mmol/l
Na+ 132
Ca++ 1,25
Mg++ 0,25
Cl- 95
C3H5O3- 40
Free from Bacterial Endotoxins Do not use unless solution is clear
Do not store above 25°C For immediate use Discard any unused
solution Not for intravenous infusion For intraperitoneal infusion
Keep out of reach and sight of children PA 167/84/11
Baxter Healthcare LtdPOM PL 00116/0231
Caxton Way Thetford Norfolk IP24 3SE UK MA 161/01105
Pyrogeenvrij Uitsluitend gebruiken indien de oplossing helder is en de zak onbeschadigd
Niet-gebruikte oplossingen vernietigen Voor intraperitoneaal gebruik
Buiten het bereik en uit het zicht van kinderen bewaren Voor gebruik de bijsluiter lezen
Niet bewaren boven 25°C Niet invriezen
Baxter BV NL-3542 CE Utrecht UR RVG 12610
Baxter SA B-7860 Lessines Op medisch voorschrift 395IS131F12
Apyrogène N’utiliser que si la solution est limpide et que si la poche
n’est pas endommagée Eliminer toute solution non utilisée
Ne pas réutiliser Ne pas administrer par voie intraveineuse
Uniquement par voie intrapéritonéale Tenir hors de la portée et de la
vue des enfants Lire la notice avant utilisation
Ne pas conserver au-dessus de 25°C Ne pas congeler
Titulaire Baxter SAS 6 av L Pasteur F-78310 Maurepas
- Médicament autorisé n° 3400936633797
Médicament non soumis à prescription médicale
Baxter SA B-7860 Lessines
Sur prescription médicale 395IS131F12
Pyrogenfrei Nur klare Lösungen in unversehrten Behältnissen verwenden
Restmengen verwerfen Nicht zur intravenösen Infusion Zur intraperitonealen Infusion Gebrauchsinformation beachten Nicht über 25°C lagern
Für Kinder unzugänglich aufbewahren Nicht einfrieren Nur zum Einmalgebrauch
Zulassungsinhaber in Belgien:
Baxter SA B-7860 Lessines Rezeptpflichtig 395IS131F12
Für Kinder unzugänglich und nicht sichtbar aufbewahren
Vertrieb/Distribution:
Baxter AG CH-8604 Volketswil Zul-Nr/N° AMM: 52799 112 B SWISSmedic Logo
Apirógeno No usar si la solución no está transparente
Desechar el resto de solución no utilizada No usar por vía intravenosa
Para administración intraperitoneal
Manténgase fuera del alcance y de la vista de los niños
Baxter SL
Pouet de Camilo 2 46394 Ribarroja del Turia (Valencia)
- 646471
Pyrogenfrei Achtung: Dieses Arzneimittel kann die Reaktionsfähigkeit und
Verkehrstüchtigkeit beeinträchtigen Nur klare Lösungen in unversehrten
Behältnissen verwenden Restmengen verwerfen Nicht zur intravenösen Infusion
Zur intraperitonealen Anwendung Arzneimittel für Kinder unzugänglich aufbewahren
Packungsbeilage beachten Rezept- und apothekenpflichtig Nicht über 25°C lagern
In der Originalverpackung aufbewahren Enizelbeutel mit Luer-Konnektor
Pharmazeutischer Unternehmer: Baxter Healthcare GmbH 1020 Wien Z Nr 1-21585
Pyrogeeniton Älä käytä ellei liuos ole kirkas
Hävitä käyttämättä jäänyt liuos Ei laskimoinfuusioon
Intraperitoneaaliseen käyttöön Ei lasten ulottuville eikä näkyville
Baxter Oy FIN-00381 Helsinki MTnr 11087 FIN
Pyrogenfri Anvendes kun hvis væsken er klar Ikke anvendt væske skal kasseres
Ikke til indtravenøs brug Til intraperitoneal brug Opbevares utilgængeligt for børn
Baxter A/S DK-3450 Allerød MTnr 14646 DK
Pyrogenfri Användes endast om vätskan är klar
Oanvänd vätska kasseras Ej för intravenöst bruk
För intraperitonealt bruk Förvaras oåtkomligt för barn
Baxter Medical AB SE-164 94 Kista MTnr 11439 SE
Mη πυρετoγóνo Mη χρησιμoπoιεíτε εκτóς εάν τo διάλυμα εíναι διαυγές και o περιέκτης δεν έχει
υπoστεí ζημιά Φυλάσσεται σε θερμοκρασία μικρότερη των 25°C Aπoρρíψτε την αχρησιμoπoíητη πoσóτητα Όχι για ενδoφλέβια έγχυση Για ενδoπεριτoναϊκή έγχυση Φυλάσσεται σε μέρος το οποίο
δεν βλέπουν και δεν προσεγγίζουν τα παιδιά Móνo για Noσoκoμειακή χρήση
Κάτοχος Αδείας Κυκλοφορίας Baxter S p A Piazzale dell’ Industria 20 IT-00144 Roma Italy
Αρ Αδεíας Κυκλoφoρíας: 40852/14-09-2009
TRK500201 B
CB-35-03-352
-
Dianeal PD4 Glucose 2.27% w/v p/v 22,7 mg/ml
5000 ml x 2 SPB5225RC Vnr 06 25 54
Solutio ad dialysis peritonealis usum praeparata/Solution for Peritoneal Dialysis/
Solution pour dialyse péritonéale en poche/Oplossing voor peritoneale dialyse/
Peritonealdialyselösung/Peritonealdialysvätska/Peritoneaalidialyysineste/
Διάλυμα Περιτοναϊκής Διαπίδυσης (Κάθαρσης)
Formula / Formule / 1000 ml enthalten / Samenstelling per 1000 ml /
1000 ml contém /Σύνθεση ανά 1000 – g/l
Dextrosum (Glucosum) Anhydricum/Anhydrous Glucose/Glucose
anhydre/Glucose anidra/Glucose wasserfrei/Watervrije glucose – 22,7 g
Natrii Chloridum/Sodium Chloride/Chlorure de Sodium/
Natriumchlorid/Cloreto de Sódio/Natriumchloride – 5,38 g
Natrii Lactas/Sodium Lactate/Lactate de Sodium/
Natrium L(+) Laktat/Lactato de sódio/Natriumlactaat – 4,48 g
Calcii Chloridum/Calcium Chloride/Chlorure de Calcium dihydraté/
Calciumchlorid·2H O/Cloreto de Cálcio/Calciumchloridedihydraat – 0,184 g
Magnesii Chloridum/Magnesium Chloride/Chlorure de Magnésium
hexahydraté/Magnesiumchlorid·6H O/Cloreto de Magnésio/
Magnesiumchloridehexahydraat – 0,051 g
Aqua ad iniectabilia/Water for Injections ad/eau ppi/to 1000 ml/
Aq. ad iniect. ad 1000 ml/Wasser für Injektionszwecke ad 1000 ml/
Água para Injectáveis qb 1000 ml/Water voor injecties ad 1000 ml
PA 167/84/11
PL 00116/0231
MA 161/01105
Z.Nr.: 1-21585
RVG 12610
395IS131F12
MTnr 11439 SE
MTnr 11087 FIN
Médicament autorisé
n° 3400936633797
Αρ. Αδείας Κυκλοφορίας:
40852/14-09-2009
Zur intraperitonealen Anwendung. Packungsbeilage beachten.
Arzneimittel für Kinder unzugänglich aufbewahren. Achtung.
Dieses Arzneimittel kann die Reaktionsfähigkeit und Verkehrstüchtiglkeit
beeinträchtigen. Nur klare Lösungen in unversehrten. Behältnissen verwenden.
Restmengen verwerfen. Nicht zur intravenösen Infusion.
Pharmazeutischer Unternehmer: Baxter Healthcare GmbH, 1020 Wien.
rezept- und apothekenpflichtig. Steril, pyrogenfrei.
France: Médicament non soumis à prescription médicale
BE : Sur prescription médicale. Op medisch voorschrift. Rezeptpflichtig.
NL : U.R.
Παρτίδα:
Lot/Ch.B.:
Λήξη
Exp./Pérempt/
Val./Verw.bis/
Utg.dat.:
Max. 25°C
Do not store above 25°C
Nicht über 25°C lagern
In der Originalverpackung aufbewahren
Ne pas conserver au-dessus de 25°C
Säilytä alle 25°C
Bewaren beneden 25°C
Förvaras under 25°C
m/Skruvkoppling
Kierrekytkentä
Single bag with Luer connector
Einzelbeutel mit Luer-Konnektor
Poche simple - Connecteur luer
Enkele zak met luer-connector
Movός σάκος - Σύνδεσμος Luer
Zul.-Nr./N° AMM.:
52799 112
88-46-11-841
Bar Code
7 046260 625549
Bar Code
(01)03400936633797 (17)000000 (10)??????????
Vnr 06 24 54
Dianeal PD4 Glucose
2.27% w/v p/v 22,7 mg/ml
Παρτίδα:
Lot/Ch.B.:
SPB5225RC
5000 ml x 2
PACKAGE/LABEL PRINCIPAL DISPLAY PANEL
Lot / Ch B / Παρτίδα Exp / Pérempt / Caducidad / Val / Utg dat / Udløbsdato / Verw bis / Λήξη
BaxterB5235R STERILE 5000 ml
DIANEAL PD4 3,86% w/v / 38,6 mg/ml Max 25°C
Glucose
Glucosa
Solutio ad dialysis peritonealis usum praeparata
Solution for Peritoneal Dialysis
Solution pour dialyse péritonéale en poche
Oplossing voor peritoneale dialyse
Peritonealdialyselösung
Peritonealdialysvätska
Peritonealdialysevæske, opløsning
Peritoneaalidialyysineste
Solución para Diálisis Peritoneal
Διάλυμα Περιτοναϊκής Διαπίδυσης (Κάθαρσης)
Formula / Formule / 1000 ml enthalten / Samenstelling per 1000 ml /
Composición por 1000 ml / Σύνθεση ανά 1000 ml g/l
Dextrosum (Glucosum) Anhydricum / Anhydrous Glucose / Glucose anhydre /
Glucosa anhidra / Glucose wasserfrei / Watervrije glucose C6H12O6 38,6 g
Natrii Chloridum / Sodium Chloride / Chlorure de Sodium / Natriumchlorid /
Cloruro Sódico / Natriumchloride NaCl 5,38 g
Natrii Lactas / Sodium Lactate / Lactate de Sodium / Natrium L (+) Lactat / Lactato Sódico /
Natriumlactaat C3H5NaO3 4,48 g
Calcii Chloridum / Calcium Chloride / Chlorure de Calcium dihydraté / Calciumchlorid • 2H2O /
Cloruro Cálcico 2H2O / Calciumchloridedihydraat CaCl2·2H2O 0,184 g
Magnesii Chloridum / Magnesium Chloride / Chlorure de Magnésium hexahydraté /
Magnesiumchlorid • 6H2O / Cloruro Magnésico 6H2O / Magnesiumchloridehexahydraat
MgCl2·6H2O 0,051 g
Aqua ad iniectabilia / Water for Injections ad / eau pour préparations injectables qsp 1000 ml / to 1000 ml / Agua para inyección cs /
Aq ad iniect ad 1000 ml / Wasser für Injektionszwecke ad 1000 ml / Water voor injecties ad 1000 ml
Osmolarity / Osmolarité /
Osmolaridad / Osmolaridade /
berechnete Osmolarität / Osmolarit / Osmolariteit /
Ωσμωτικότητα 483 mOsm/l
mmol/l
Na+ 132
Ca++ 1,25
Mg++ 0,25
Cl- 95
C3H5O3- 40
Free from Bacterial Endotoxins Do not use unless solution is clear
Do not store above 25°C For immediate use Discard any unused
solution Not for intravenous infusion For intraperitoneal infusion
Keep out of reach and sight of children PA 167/84/21
Baxter Healthcare LtdPOM PL 00116/0232
Caxton Way Thetford Norfolk IP24 3SE UK MA 161/01106
Pyrogeenvrij Uitsluitend gebruiken indien de oplossing helder is en de zak onbeschadigd
Niet-gebruikte oplossingen vernietigen Voor intraperitoneaal gebruik
Buiten het bereik en uit het zicht van kinderen bewaren Voor gebruik de bijsluiter lezen
Niet bewaren boven 25°C Niet invriezen
Baxter BV NL-3542 CE Utrecht UR RVG 12611
Baxter SA B-7860 Lessines Op medisch voorschrift 395IS134F12
Apyrogène N’utiliser que si la solution est limpide et que si la poche
n’est pas endommagée Eliminer toute solution non utilisée
Ne pas réutiliser Ne pas administrer par voie intraveineuse
Uniquement par voie intrapéritonéale Tenir hors de la portée et de la
vue des enfants Lire la notice avant utilisation
Ne pas conserver au-dessus de 25°C Ne pas congeler
Titulaire Baxter SAS 6 av L Pasteur F-78310 Maurepas
- Médicament autorisé n° 3400936636750
Médicament non soumis à prescription médicale
Baxter SA B-7860 Lessines
Sur prescription médicale 395IS134F12
Pyrogenfrei Nur klare Lösungen in unversehrten Behältnissen verwenden
Restmengen verwerfen Nicht zur intravenösen Infusion Zur intraperitonealen Infusion Gebrauchsinformation beachten Nicht über 25°C lagern
Für Kinder unzugänglich aufbewahren Nicht einfrieren Nur zum Einmalgebrauch
Zulassungsinhaber in Belgien:
Baxter SA B-7860 Lessines Rezeptpflichtig 395IS134F12
Für Kinder unzugänglich und nicht sichtbar aufbewahren
Vertrieb/Distribution:
Baxter AG CH-8604 Volketswil Zul-Nr/N° AMM: 52799 163 B SWISSmedic Logo
Apirógeno No usar si la solución no está transparente
Desechar el resto de solución no utilizada No usar por vía intravenosa
Para administración intraperitoneal
Manténgase fuera del alcance y de la vista de los niños
Baxter SL
Pouet de Camilo 2 46394 Ribarroja del Turia (Valencia)
- 646455
Pyrogenfrei Achtung: Dieses Arzneimittel kann die Reaktionsfähigkeit und
Verkehrstüchtigkeit beeinträchtigen Nur klare Lösungen in unversehrten
Behältnissen verwenden Restmengen verwerfen Nicht zur intravenösen Infusion
Zur intraperitonealen Anwendung Arzneimittel für Kinder unzugänglich aufbewahren
Packungsbeilage beachten Rezept- und apothekenpflichtig Nicht über 25°C lagern
In der Originalverpackung aufbewahren Enizelbeutel mit Luer-Konnektor
Pharmazeutischer Unternehmer: Baxter Healthcare GmbH 1020 Wien Z Nr 1-21584
Pyrogeeniton Älä käytä ellei liuos ole kirkas
Hävitä käyttämättä jäänyt liuos Ei laskimoinfuusioon
Intraperitoneaaliseen käyttöön Ei lasten ulottuville eikä näkyville
Baxter Oy FIN-00381 Helsinki MTnr 11087 FIN
Pyrogenfri Anvendes kun hvis væsken er klar Ikke anvendt væske skal kasseres
Ikke til indtravenøs brug Til intraperitoneal brug Opbevares utilgængeligt for børn
Baxter A/S DK-3450 Allerød MTnr 14647 DK
Pyrogenfri Användes endast om vätskan är klar
Oanvänd vätska kasseras Ej för intravenöst bruk
För intraperitonealt bruk Förvaras oåtkomligt för barn
Baxter Medical AB SE-164 94 Kista MTnr 11440 SE
Mη πυρετoγóνo Mη χρησιμoπoιεíτε εκτóς εάν τo διάλυμα εíναι διαυγές και o περιέκτης δεν έχει
υπoστεí ζημιά Φυλάσσεται σε θερμοκρασία μικρότερη των 25°C Aπoρρíψτε την αχρησιμoπoíητη πoσóτητα Όχι για ενδoφλέβια έγχυση Για ενδoπεριτoναϊκή έγχυση Φυλάσσεται σε μέρος το οποίο
δεν βλέπουν και δεν προσεγγίζουν τα παιδιά Móνo για Noσoκoμειακή χρήση
Κάτοχος Αδείας Κυκλοφορίας Baxter S p A Piazzale dell’ Industria 20 IT-00144 Roma Italy
Αρ Αδεíας Κυκλoφoρíας: 40855/14-09-2009
TRK500204 B
CB-35-03-353
-
Dianeal PD4 Glucose 3.86% w/v p/v 38,6 mg/ml
5000 ml x 2 SPB5235RC Vnr 06 25 62
Solutio ad dialysis peritonealis usum praeparata/Solution for Peritoneal Dialysis/
Solution pour dialyse péritonéale en poche/Oplossing voor peritoneale dialyse/
Peritonealdialyselösung/Peritonealdialysvätska/Peritoneaalidialyysineste/
Διάλυμα Περιτοναϊκής Διαπίδυσης (Κάθαρσης)
Formula / Formule / 1000 ml enthalten / Samenstelling per 1000 ml /
1000 ml contém /Σύνθεση ανά 1000 – g/l
Dextrosum (Glucosum) Anhydricum/Anhydrous Glucose/Glucose
anhydre/Glucose anidra/Glucose wasserfrei/Watervrije glucose – 38,6 g
Natrii Chloridum/Sodium Chloride/Chlorure de Sodium/
Natriumchlorid/Cloreto de Sódio/Natriumchloride – 5,38 g
Natrii Lactas/Sodium Lactate/Lactate de Sodium/
Natrium L(+) Laktat/Lactato de sódio/Natriumlactaat – 4,48 g
Calcii Chloridum/Calcium Chloride/Chlorure de Calcium dihydraté/
Calciumchlorid·2H O/Cloreto de Cálcio/Calciumchloridedihydraat – 0,184 g
Magnesii Chloridum/Magnesium Chloride/Chlorure de Magnésium
hexahydraté/Magnesiumchlorid·6H O/Cloreto de Magnésio/
Magnesiumchloridehexahydraat – 0,051 g
Aqua ad iniectabilia/Water for Injections ad/eau ppi/to 1000 ml/
Aq. ad iniect. ad 1000 ml/Wasser für Injektionszwecke ad 1000 ml/
Água para Injectáveis qb 1000 ml/Water voor injecties ad 1000 ml
PA 167/84/21
PL 00116/0232
MA 161/01106
Z.Nr.: 1-21584
RVG 12611
395IS131F12
MTnr 11440 SE
MTnr 11088 FIN
Médicament autorisé
n° 3400936636750
Αρ. Αδείας Κυκλοφορίας:
40855/14-09-2009
Zur intraperitonealen Anwendung. Packungsbeilage beachten.
Arzneimittel für Kinder unzugänglich aufbewahren. Achtung.
Dieses Arzneimittel kann die Reaktionsfähigkeit und Verkehrstüchtiglkeit
beeinträchtigen. Nur klare Lösungen in unversehrten. Behältnissen verwenden.
Restmengen verwerfen. Nicht zur intravenösen Infusion.
Pharmazeutischer Unternehmer: Baxter Healthcare GmbH, 1020 Wien.
rezept- und apothekenpflichtig. Steril, pyrogenfrei.
France: Médicament non soumis à prescription médicale
BE : Sur prescription médicale. Op medisch voorschrift. Rezeptpflichtig.
NL : U.R.
Παρτίδα:
Lot/Ch.B.:
Λήξη
Exp./Pérempt/
Val./Verw.bis/
Utg.dat.:
Max. 25°C
Do not store above 25°C
Nicht über 25°C lagern
In der Originalverpackung aufbewahren
Ne pas conserver au-dessus de 25°C
Säilytä alle 25°C
Bewaren beneden 25°C
Förvaras under 25°C
m/Skruvkoppling
Kierrekytkentä
Single bag with Luer connector
Einzelbeutel mit Luer-Konnektor
Poche simple - Connecteur luer
Enkele zak met luer-connector
Movός σάκος - Σύνδεσμος Luer
Zul.-Nr./N° AMM.:
52799 163
88-46-11-842
Bar Code
7 046260 625624
Bar Code
(01)03400936636750 (17)000000 (10)??????????
Vnr 06 25 62
Dianeal PD4 Glucose
3.86% w/v p/v 38,6 mg/ml
Παρτίδα:
Lot/Ch.B.:
SPB5225RC
5000 ml x 2
| DIANEAL FOR PERITONEAL DIALYSIS
anhydrouse dextrose, sodium chloride, sodium lactate, calcium chloride, magnesium chloride injection, solution |
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|||||||||||||||||||||
| DIANEAL FOR PERITONEAL DIALYSIS
anhydrous dextrose, sodium chloride, sodium lactate, calcium chloride, magnesium chloride injection, solution |
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|||||||||||||||||||||
| DIANEAL FOR PERITONEAL DIALYSIS
anhydrous dextrose, sodium chloride, sodium lactate, calcium chloride, magnesium chloride injection, solution |
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|||||||||||||||||||||
| Labeler - Baxter Healthcare Corporation (005083209) |
| Establishment | |||
| Name | Address | ID/FEI | Business Operations |
|---|---|---|---|
| Baxter Healthcare S.A. | 988899845 | ANALYSIS(0941-0464, 0941-0465, 0941-0466) , MANUFACTURE(0941-0464, 0941-0465, 0941-0466) , LABEL(0941-0464, 0941-0465, 0941-0466) , STERILIZE(0941-0464, 0941-0465, 0941-0466) | |